Unsere Hauptprodukte: Aminosilikon, Blocksilikon, hydrophiles Silikon, alle ihre Silikonemulsionen, Benetzungs- und Reibechtheitsverbesserer, wasserabweisende Mittel (fluorfrei, Kohlenstoff 6, Kohlenstoff 8), Demin-Waschchemikalien (ABS, Enzym, Spandex-Schutz, Mangan-Entferner), weitere Einzelheiten erhalten Sie unter: Mandy +86 19856618619 (Whatsapp)
Einführung in Tenside
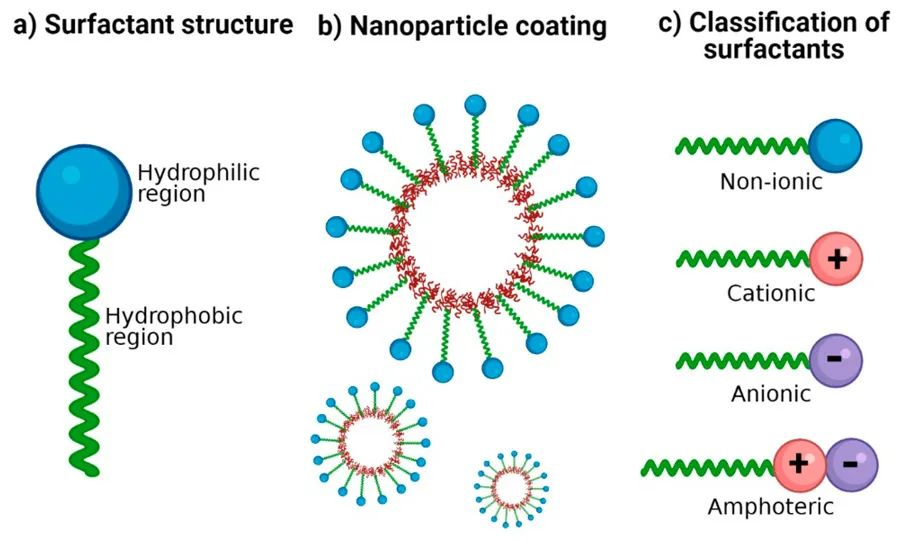
Tenside besitzen eine amphiphile Molekülstruktur: Ein Ende enthält eine hydrophile Gruppe, den sogenannten hydrophilen Kopf, während das andere Ende eine hydrophobe Gruppe, den sogenannten hydrophoben Schwanz, enthält. Der hydrophile Kopf ermöglicht es den Tensiden, sich in ihrer Monomerform in Wasser aufzulösen.
Bei der hydrophilen Gruppe handelt es sich häufig um eine polare Gruppe. Beispiele für polare hydrophile Gruppen sind beispielsweise eine Carboxylgruppe (-COOH), eine Sulfonsäuregruppe (-SO3H), eine Aminogruppe (-NH2), Amine und deren Salze, Hydroxylgruppen (-OH), Amidgruppen oder Etherbindungen (-O-).
Bei der hydrophoben Gruppe handelt es sich typischerweise um eine unpolare Kohlenwasserstoffkette, wie etwa hydrophobe Alkylketten (R- für Alkyl) oder aromatische Gruppen (Ar- für Aryl).
Tenside lassen sich in ionische Tenside (einschließlich kationischer und anionischer Tenside), nichtionische Tenside, amphotere Tenside, gemischte Tenside und weitere einteilen. In Tensidlösungen bilden die Tensidmoleküle ab einer bestimmten Tensidkonzentration verschiedene geordnete Aggregate, sogenannte Mizellen. Der Prozess der Mizellbildung ist eine entscheidende grundlegende Eigenschaft von Tensidlösungen, da viele wichtige Grenzflächenphänomene mit der Mizellenbildung verbunden sind.
Die Konzentration, bei der Tenside in Lösung Mizellen bilden, wird als kritische Mizellenkonzentration (CMC) bezeichnet. Mizellen sind keine festen, kugelförmigen Strukturen, sondern weisen extreme Unregelmäßigkeiten und dynamische Formänderungen auf. Unter bestimmten Bedingungen können Tenside auch umgekehrte Mizellenzustände aufweisen.
Faktoren, die CMC beeinflussen:
- Struktur des Tensids
- Art und Vorhandensein von Zusatzstoffen
- Temperatur
Wechselwirkungen zwischen Tensiden und Proteinen
Proteine enthalten unpolare, polare und geladene Gruppen, und viele amphiphile Moleküle können auf verschiedene Weise mit Proteinen interagieren. Je nach Bedingungen können Tenside molekular organisierte Aggregate mit unterschiedlichen Strukturen bilden, wie z. B. Mizellen oder umgekehrte Mizellen, die unterschiedlich mit Proteinen interagieren.
Die Wechselwirkungen zwischen Proteinen und Tensiden (Protein-Tensid, PS) beinhalten hauptsächlich elektrostatische und hydrophobe Wechselwirkungen. Ionische Tenside interagieren mit Proteinen hauptsächlich über die elektrostatischen Kräfte der polaren Gruppe und die hydrophoben Wechselwirkungen der aliphatischen Kohlenstoffkette. Sie binden an die polaren und hydrophoben Bereiche des Proteins und bilden so PS-Komplexe.
Nichtionische Tenside interagieren mit Proteinen hauptsächlich über hydrophobe Kräfte, wobei die hydrophoben Ketten mit den hydrophoben Bereichen der Proteine interagieren. Diese Wechselwirkung kann sowohl die Struktur als auch die Funktion des Tensids und des Proteins beeinflussen. Daher bestimmen Art und Konzentration der Tenside sowie der Umgebungskontext, ob Tenside Proteine stabilisieren oder destabilisieren und ob sie die Aggregation oder Dispersion fördern.
HLB-Wert von Tensiden
Damit ein Tensid seine einzigartige Grenzflächenaktivität entfalten kann, muss es ein Gleichgewicht zwischen hydrophoben und hydrophilen Komponenten aufweisen. Der HLB-Wert (Hydrophile-Lipophile Balance) ist ein Maß für das hydrophile-lipophile Gleichgewicht von Tensiden und dient als Indikator für die hydrophilen und hydrophoben Eigenschaften der Tenside.
Der HLB-Wert ist ein relativer Wert (zwischen 0 und 40). Paraffin hat beispielsweise einen HLB-Wert von 0 (keine hydrophile Komponente), Polyethylenglykol einen HLB-Wert von 20 und das stark hydrophile SDS (Natriumdodecylsulfat) einen HLB-Wert von 40. Der HLB-Wert kann als Orientierungshilfe bei der Auswahl von Tensiden dienen. Ein höherer HLB-Wert weist auf eine bessere Hydrophilie hin, während ein niedrigerer HLB-Wert auf eine schlechtere Hydrophilie hindeutet.
Veröffentlichungszeit: 10. September 2024

