

Die Schrumpfkraft jeder Einheitslänge auf der Flüssigkeitsoberfläche wird als Oberflächenspannung bezeichnet und die Einheit ist N. · m-1.

Die Eigenschaft der Reduzierung der Oberflächenspannung des Lösungsmittels wird als Oberflächenaktivität bezeichnet und eine Substanz mit dieser Eigenschaft wird als oberflächenaktive Substanz bezeichnet.
Die oberflächenaktive Substanz, die Moleküle in wässriger Lösung binden und Mizellen und andere Assoziationen bilden kann und eine hohe Oberflächenaktivität aufweist, während gleichzeitig Benetzung, Emulgierung, Schäumen, Waschen usw. Tensid bezeichnet wird.
Tensid sind organische Verbindungen mit besonderer Struktur und Eigenschaft, die die Grenzflächenspannung zwischen zwei Phasen oder der Oberflächenspannung von Flüssigkeiten (im Allgemeinen Wasser) mit Benetzung, Schäumen, Emulsifizierung, Waschen und anderen Eigenschaften erheblich verändern können.
In Bezug auf die Struktur haben Tenside ein gemeinsames Merkmal, als sie zwei Gruppen unterschiedlicher Natur in ihren Molekülen enthalten. An einem Ende befindet sich eine lange Kette unpolarer Gruppe, die in Öl und unlöslich in Wasser löslich ist und auch als hydrophobe Gruppe oder wasserabweisende Gruppe bezeichnet wird. Eine solche wasserabweisende Gruppe besteht im Allgemeinen lange Ketten von Kohlenwasserstoffen, manchmal auch für organische Fluor, Silizium, Organophosphat, Organotinkette usw. Am anderen Ende befindet sich eine wasserlösliche Gruppe, eine hydrophile Gruppe oder ölabrechnungswichtige Gruppe. Die hydrophile Gruppe muss ausreichend hydrophil sein, um sicherzustellen, dass ganze Tenside in Wasser löslich sind und über die notwendige Löslichkeit verfügen. Da Tenside hydrophile und hydrophobe Gruppen enthalten, können sie in mindestens einer der flüssigen Phasen löslich sein. Diese hydrophile und lipophile Eigenschaft von Tensid wird als Amphiphilizität bezeichnet.


Tensid ist eine Art amphiphile Moleküle mit hydrophoben und hydrophilen Gruppen. Hydrophobe Gruppen von Tensiden bestehen im Allgemeinen aus langkettigen Kohlenwasserstoffen wie dem geraden Alkyl C8 ~ C20, dem Alkyl C8 ~ C20 , Alkylphenyl (Alkylkohlenstoff-Tom) und 8 bis 16) und dergleichen. Der Unterschied, der zwischen hydrophoben Gruppen klein ist, liegt hauptsächlich in den strukturellen Veränderungen von Kohlenwasserstoffketten. Und die Arten von hydrophilen Gruppen sind mehr, daher hängen die Eigenschaften von Tensiden hauptsächlich mit hydrophilen Gruppen zusammen, zusätzlich zur Größe und Form der hydrophoben Gruppen. Die strukturellen Veränderungen hydrophiler Gruppen sind größer als die von hydrophoben Gruppen, daher basiert die Klassifizierung von Tensiden im Allgemeinen auf der Struktur hydrophiler Gruppen. Diese Klassifizierung basiert darauf, ob die hydrophile Gruppe ionisch ist oder nicht, und sie ist in anionische, kationische, nichtionische, zwitterionische und andere spezielle Arten von Tensiden unterteilt.

① Adsorption von Tensiden am Interfac
Tensidmoleküle sind amphiphile Moleküle mit lipophilen und hydrophilen Gruppen. Wenn das Tensid in Wasser aufgelöst wird, wird seine hydrophile Gruppe von Wasser angezogen und in Wasser auflöst, während seine lipophile Gruppe durch Wasser abgestoßen wird und Wasser verlässt, was zur Adsorption von Tensidmolekülen (oder Ionen) an der Grenzfläche der beiden Phasen führt. Je mehr Tensidmoleküle (oder Ionen) an der Grenzfläche adsorbiert werden, desto größer ist die Verringerung der Grenzflächenspannung.
② Einige Eigenschaften der Adsorptionsmembran
Oberflächendruck der Adsorptionsmembran: Tensidadsorption an der Gas-Flüssigkeits-Grenzfläche zur Bildung einer Adsorptionsmembran, wie z.
Oberflächenviskosität: Wie Oberflächendruck ist eine Oberflächenviskosität eine Eigenschaft, die durch unlösliche molekulare Membran zeigt. Aufgehängt durch einen Platinring des feinen Metalldrahtes, so dass seine Ebene die Wasseroberfläche des Tanks kontaktiert, drehen Sie den Platinring, den Platinring durch die Viskosität des Wasserhinderung, die Amplitude zerlegt allmählich, nach der die Oberflächenviskosität gemessen werden kann. Die Methode ist: Zuerst wird das Experiment auf der reinen Wasseroberfläche durchgeführt, um den Abfall der Amplitude zu messen, und dann wird der Zerfall nach der Bildung der Oberflächenmembran gemessen und die Viskosität der Oberflächenmembran aus der Differenz zwischen den beiden abgeleitet.
Die Oberflächenviskosität ist eng mit der Solidität der Oberflächenmembran verwandt, und da die Adsorptionsmembran Oberdruck und Viskosität aufweist, muss sie Elastizität aufweisen. Je höher der Oberflächendruck und desto höher die Viskosität der adsorbierten Membran, desto höher sein elastisches Modul. Der elastische Modul der Oberflächenadsorptionsmembran ist im Prozess der Blasenstabilisierung wichtig.
③ Bildung von Mizellen
Verdünnte Lösungen von Tensiden befolgen die Gesetze, die von idealen Lösungen gefolgt sind. Die Menge an Tensid, die auf der Oberfläche der Lösung adsorbiert ist, nimmt mit der Konzentration der Lösung zu, und wenn die Konzentration einen bestimmten Wert erreicht oder übersteigt, steigt die Menge an Adsorption nicht mehr, und diese überschüssigen Tensidmoleküle sind auf zufällige Weise oder auf eine regelmäßige Weise in der Lösung. Sowohl Praxis als auch Theorie zeigen, dass sie Assoziationen in Lösung bilden, und diese Assoziationen werden als Mizellen bezeichnet.
Kritische Mizellenkonzentration (CMC): Die minimale Konzentration, bei der Tenside Mizellen in Lösung bilden, wird als kritische Mizellenkonzentration bezeichnet.
④ CMC -Werte gemeinsamer Tenside.

HLB ist die Abkürzung des hydrophilen lipophilen Gleichgewichts, das den hydrophilen und lipophilen Gleichgewicht der hydrophilen und lipophilen Gruppen des Tensids, dh den HLB -Wert des Tensids, anzeigt. Ein großer HLB -Wert zeigt ein Molekül mit starker Hydrophilie und schwacher Lipophilie an; Umgekehrt starke Lipophilie und schwache Hydrophilie.
① Bestimmungen des HLB -Werts
Der HLB-Wert ist ein relativer Wert. Wenn der HLB-Wert als Standard entwickelt wird, wird der HLB-Wert von Paraffin-Wachs, der keine hydrophilen Eigenschaften aufweist, zu 0, während der HLB-Wert von Natriumdodecylsulfat, der Wasserflecken ist, im Allgemeinen. Der HLB-Wert von HLB-Wert ist im Allgemeinen. Der HLB-Wert ist im Allgemeinen. Der HLB-Wert ist im Allgemeinen. Der HLB-Wert. Der HLB-Wert ist im Allgemeinen. Der HLB-Wert ist allgemein. Weniger als 10 sind lipophil, während diejenigen mehr als 10 hydrophil sind. Somit beträgt der Wendepunkt von lipophil zu hydrophil etwa 10.
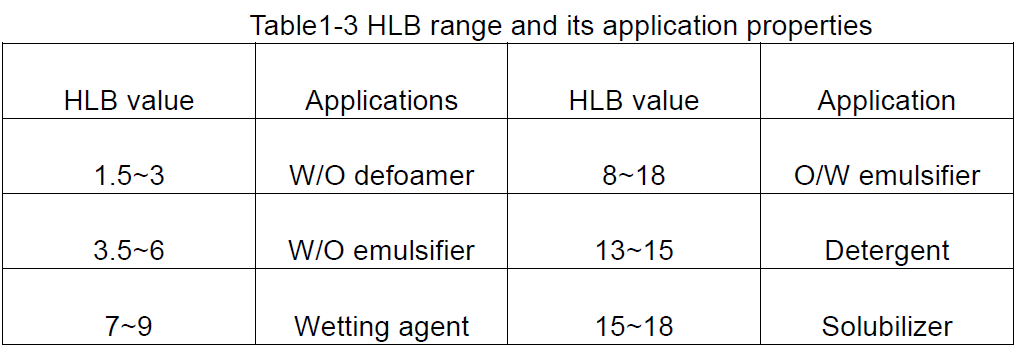
Basierend auf den HLB-Werten von Tensiden kann eine allgemeine Vorstellung ihrer möglichen Verwendungen erhalten werden, wie in Tabelle 1-3 gezeigt.

Zwei gegenseitig unlösliche Flüssigkeiten, die in den anderen als Partikel (Tröpfchen oder Flüssigkristalle) ein System bilden, das als Emulsion bezeichnet wird. Dieses System ist aufgrund der Zunahme der Grenzfläche der beiden Flüssigkeiten thermodynamisch instabil, wenn die Emulsion gebildet wird. Um die Emulsion stabil zu machen, müssen eine dritte Komponente - Emulgatoren - die Grenzflächenenergie des Systems reduziert werden. Der Emulgator gehört zum Tensid, seine Hauptfunktion besteht darin, die Rolle der Emulsion zu spielen. Die Phase der Emulsion, die als Tröpfchen existiert, wird als dispergierte Phase (oder innere Phase, diskontinuierliche Phase) bezeichnet, und die andere miteinander verbundene andere Phase wird als Dispersionsmedium (oder äußere Phase, kontinuierliche Phase) bezeichnet.
① Emulgatoren und Emulsionen
Häufige Emulsionen, eine Phase ist Wasser oder wässrige Lösung, die andere Phase ist organische Substanzen, die nicht mit Wasser mischbar sind, wie Fett, Wachs usw. Die durch Wasser und Öl gebildete Emulsion kann gemäß ihrer Dispersionssituation unterteilt werden. Komplexe Wasser-in-Wasser-W/O/W-Art und Öl-in-Wasser-In-Öl-O/W/O-Typ-Multi-Emulsionen können ebenfalls gebildet werden.
Emulgatoren werden verwendet, um Emulsionen zu stabilisieren, indem die Grenzflächenspannung reduziert und einmolekulare Grenzflächenmembran bildet.
Bei der Emulgierung der Emulgatoranforderungen:
A: Der Emulgator muss in der Lage sein, die Grenzfläche zwischen den beiden Phasen zu adsorbieren oder zu bereichern, so dass die Grenzflächenspannung verringert wird.
B: Der Emulgator muss der Ladung die Partikel geben, so dass die elektrostatische Abstoßung zwischen den Partikeln oder eine stabile, hochviskose Schutzmembran um die Partikel bildet.
Daher muss die als Emulgatoren verwendete Substanz amphiphile Gruppen zur Emulifizierung haben, und Tenside können diese Anforderung erfüllen.
② Vorbereitungsmethoden von Emulsionen und Faktoren, die die Stabilität von Emulsionen beeinflussen
Es gibt zwei Möglichkeiten, Emulsionen vorzubereiten: Eine besteht darin, die mechanische Methode zu verwenden, um die Flüssigkeit in winzigen Partikeln in einer anderen Flüssigkeit zu zerstreuen, die hauptsächlich in der Industrie zur Herstellung von Emulsionen verwendet wird; Das andere besteht darin, die Flüssigkeit in einem molekularen Zustand in einer anderen Flüssigkeit aufzulösen und sich dann richtig zu sammeln, um Emulsionen zu bilden.
Die Stabilität einer Emulsion ist die Fähigkeit zur Anti-Partikel-Aggregation, die zu einer Phasentrennung führt. Emulsionen sind thermodynamisch instabile Systeme mit großer freier Energie. Daher ist die sogenannte Stabilität einer Emulsion tatsächlich die Zeit, die das System zum Erreichen des Gleichgewichts erfordert, dh die Zeit, die für die Trennung einer der Flüssigkeiten im System erforderlich ist.
Wenn die Grenzflächenmembran mit Fettalkoholen, Fettsäuren und Fettaminen und anderen polaren organischen Molekülen signifikant höher ist. Dies liegt daran, dass in der Grenzflächen -Adsorptionsschicht von Emulgatormolekülen und Alkoholen, Säuren und Aminen und anderen polaren Molekülen eine "Komplex" bildet, so dass die Grenzflächenmembranfestigkeit zunahm.
Emulgatoren, die aus mehr als zwei Tensiden bestehen, werden als gemischte Emulgatoren bezeichnet. Gemischter Emulgator an der Wasser/Öl -Grenzfläche; Intermolekulare Wirkung kann Komplexe bilden. Aufgrund der starken intermolekularen Wirkung wird die Grenzflächenspannung signifikant reduziert, die Menge an Emulgator, die an der Grenzfläche adsorbiert ist, erhöht sich signifikant, die Bildung der Grenzflächenmembrandichte steigt und die Stärke steigt.
Die Ladung der flüssigen Perlen hat einen signifikanten Einfluss auf die Stabilität der Emulsion. Stabile Emulsionen, deren flüssige Perlen im Allgemeinen aufgeladen sind. Wenn ein ionischer Emulgator verwendet wird, hat das an der Grenzfläche adsorbierte Emulgatrierträger seine lipophile Gruppe in die Ölphase eingeführt, und die hydrophile Gruppe befindet sich in der Wasserphase, wodurch die flüssigen Perlen geladen werden. Da die Emulsion mit der gleichen Ladung Perlen abweist, stoßen sie sich gegenseitig ab und nicht leicht zu agglomerieren, so dass die Stabilität erhöht wird. Es ist zu erkennen, dass je mehr Emulgatoren an den Perlen adsorbiert wurden, desto größer die Fähigkeit, die Perlen vor Agglomeration zu verhindern, desto stabiler ist das Emulsionssystem.
Die Viskosität des Emulsionsdispersionsmediums hat einen gewissen Einfluss auf die Stabilität der Emulsion. Je höher die Viskosität des Dispersionsmediums, desto höher ist die Stabilität der Emulsion. Dies liegt daran, dass die Viskosität des Dispersionsmediums groß ist, was sich stark auf die Brownsche Bewegung der flüssigen Perlen auswirkt und die Kollision zwischen den flüssigen Perlen verlangsamt, so dass das System stabil bleibt. Normalerweise können die Polymersubstanzen, die in Emulsionen gelöst werden können, die Viskosität des Systems erhöhen und die Stabilität von Emulsionen höher machen. Darüber hinaus können Polymere auch eine starke Grenzflächenmembran bilden, was das Emulsionssystem stabiler macht.
In einigen Fällen kann die Zugabe von festem Pulver auch dazu führen, dass die Emulsion dazu neigt, sich zu stabilisieren. Festes Pulver befindet sich in Wasser, Öl oder Grenzfläche, abhängig vom Öl, Wasser auf der Benetzungskapazität des festen Pulvers, wenn das feste Pulver nicht vollständig mit Wasser, sondern auch durch Öl nass ist, bleibt an der Wasser- und Ölschnittstelle.
Das Festpulver macht die Emulsion nicht stabil, da das an der Grenzfläche gesammelte Pulver die Grenzflächenmembran verbessert, die der Grenzflächenadsorption von Emulgatormolekülen ähnelt.
Tenside können die Löslichkeit von unlöslichen oder leicht wasserlöslichen organischen Substanzen nach der Bildung von Mizellen in wässriger Lösung erheblich erhöhen, und die Lösung ist zu diesem Zeitpunkt transparent. Dieser Effekt der Mizelle wird als Solubilisierung bezeichnet. Das Tensid, das Solubilisierung erzeugen kann, wird als Solubilizer bezeichnet, und die organische Substanz, die solubilisiert wird, wird als solubilisierte Materie bezeichnet.

Schaum spielt eine wichtige Rolle im Waschprozess. Schaum ist ein Dispersionssystem, bei dem ein Gas in flüssiger oder fester Feste mit dem Gas als dispergierter Phase und der Flüssigkeit oder des Feststoffs als Dispersionsmedium dispergiert wird, wobei der erstere als flüssiger Schaum bezeichnet wird, während der letztere als fester Schaum bezeichnet wird, z.
(1) Schaumbildung
Mit Schaum meinen wir hier ein Aggregat von Luftblasen, die durch eine flüssige Membran getrennt sind. Diese Art von Blase steigt aufgrund der großen Dichte zwischen der dispergierten Phase (Gas) und dem Dispersionsmedium (Flüssigkeit) in Kombination mit der niedrigen Viskosität der Flüssigkeit immer schnell auf die Flüssigkeitsoberfläche.
Die Bildung einer Blase besteht darin, eine große Menge Gas in die Flüssigkeit zu bringen, und die Blasen in der Flüssigkeit kehren schnell an die Oberfläche zurück und bilden ein Aggregat von Blasen, die durch eine kleine Menge Flüssiggas getrennt sind.
Schaum hat zwei signifikante Merkmale in Bezug auf die Morphologie: Eine ist, dass die Blasen als dispergierte Phase häufig eine polyedrische Form haben. Dies liegt daran, dass der Flüssigkeitsfilm an der Kreuzung der Blasen eine Tendenz gibt, dass der Flüssigkeitsfilm dünn wird, sodass die Blasen zu einer Polyeder werden, wenn der Flüssigkeitsfilm bis zu einem gewissen Grad dünn wird, und es zu Blasenrupturen zu Blasen -Ruptur ist. Die zweite ist, dass reine Flüssigkeiten keinen stabilen Schaum bilden können, die Flüssigkeit, die Schaum bilden kann, mindestens zwei oder mehr Komponenten beträgt. Wässrige Lösungen von Tensiden sind typisch für Systeme, die anfällig für die Schaumzeugung sind, und ihre Fähigkeit, Schaum zu erzeugen, hängt auch mit anderen Eigenschaften zusammen.
Tenside mit guter Schaumkraft werden als Schaummittel bezeichnet. Obwohl das Schaummittel eine gute Fähigkeit zur Schaumstoff hat, aber der gebildete Schaum möglicherweise nicht in der Lage ist, lange Zeit aufrechtzuerhalten, ist seine Stabilität nicht unbedingt gut. Um die Stabilität des Schaums aufrechtzuerhalten, häufig im Schaumstoffmittel, um Substanzen hinzuzufügen, die die Stabilität des Schaums erhöhen können, wird die Substanz als Schaumstabilisator bezeichnet. Der häufig verwendete Stabilisator ist Lauryldiethanolamin und Dodecyl -Dimethylaminoxid.
(2) Stabilität des Schaums
Schaum ist ein thermodynamisch instabiles System, und der endgültige Trend besteht darin, dass die Gesamtfläche der Flüssigkeit innerhalb des Systems nach dem Brechen der Blase abnimmt und die freie Energie abnimmt. Der Entschichtungsprozess ist der Prozess, durch den die flüssige Membran, die das Gas trennt, dicker und dünner wird, bis sie bricht. Daher wird der Grad der Stabilität des Schaums hauptsächlich durch die Geschwindigkeit der Flüssigkeitsentladung und die Festigkeit des Flüssigkeitsfilms bestimmt. Die folgenden Faktoren beeinflussen dies ebenfalls.
(3) Schaumzerstörung
Das Grundprinzip der Schaumzerstörung besteht darin, die Bedingungen zu ändern, die den Schaum erzeugen, oder um die stabilisierenden Faktoren des Schaums zu beseitigen. Daher gibt es sowohl physikalische als auch chemische Methoden der Enthüllung.
Physikalisches Ausfall bedeutet, die Bedingungen der Schaumstoffproduktion zu verändern und gleichzeitig die chemische Zusammensetzung der Schaumstofflösung beizubehalten, z. B. externe Störungen, Änderungen der Temperatur oder des Drucks und der Ultraschallbehandlung sind wirksame physikalische Methoden zur Beseitigung von Schaum.
Die chemische Enthaudmethode besteht darin, bestimmte Substanzen zur Interaktion mit dem Schaummittel hinzuzufügen, um die Festigkeit des Flüssigkeitsfilms im Schaum zu verringern und somit die Stabilität des Schaums zu verringern, um den Zweck der Entgiftung zu erreichen. Solche Substanzen werden als Entmündung bezeichnet. Die meisten Enttäuschung sind Tenside. Daher sollte entsprechend dem Mechanismus des Enthaltens eine starke Fähigkeit zur Reduzierung der Oberflächenspannung auf der Oberfläche haben, und die Wechselwirkung zwischen den Oberflächenadsorptionsmolekülen ist schwach, Adsorptionsmoleküle, die in einer lockeren Struktur angeordnet sind.
Es gibt verschiedene Arten von Enthalten, aber im Grunde sind sie alle nichtionische Tenside. Nichtionische Tenside haben Anti-Frist-Eigenschaften in der Nähe oder über ihrem Wolkenpunkt und werden häufig als Entmündung verwendet. Alkohole, insbesondere Alkohole mit Verzweigungsstruktur, Fettsäuren und Fettsäureestern, Polyamiden, Phosphatester, Silikonölen usw. werden üblicherweise auch als hervorragende Entmündung verwendet.
(4) Schaum und Waschen
Es gibt keinen direkten Zusammenhang zwischen Schaum und Waschwirksamkeit, und die Menge an Schaum zeigt nicht die Wirksamkeit der Wäsche an. Zum Beispiel haben nichtionische Tenside weitaus weniger Schaumeigenschaften als Seifen, aber ihre Dekontamination ist viel besser als Seifen.
In einigen Fällen kann der Schaum hilfreich sein, um Schmutz und Schmutz zu entfernen. Wenn Sie beispielsweise Geschirr im Haus waschen, nimmt der Schaum des Waschmittels die Öltröpfchen auf, und wenn Sie Teppiche schrubben, hilft der Schaum, Staub, Pulver und andere feste Schmutz aufzunehmen. Darüber hinaus kann Schaum manchmal als Hinweis auf die Wirksamkeit eines Waschmittels verwendet werden. Da Fettöle eine hemmende Wirkung auf den Schaum des Reinigungsmittels haben, wird bei zu viel Öl und zu wenig Reinigungsmittel kein Schaum erzeugt oder der ursprüngliche Schaum verschwindet. Schaum kann manchmal auch als Indikator für die Sauberkeit einer Spülung verwendet werden, da die Menge an Schaum in der Spülenlösung mit der Verringerung des Waschmittels abnimmt, sodass die Menge an Schaum verwendet werden kann, um den Grad der Spülung zu bewerten.
In einem breiten Sinne ist das Waschen der Prozess, unerwünschte Komponenten aus dem zu gewaschenen Objekt zu entfernen und einen Zweck zu erreichen. Das Waschen im üblichen Sinne bezieht sich auf den Prozess des Entfernens von Schmutz von der Oberfläche des Trägers. Beim Waschen wird die Wechselwirkung zwischen Schmutz und Träger durch die Wirkung einiger chemischer Substanzen (z. B. Waschmittel usw.) geschwächt oder beseitigt, so dass die Kombination von Schmutz und Träger in die Kombination von Schmutz und Reinigungsmittel und schließlich vom Träger getrennt wird. Wenn die zu entfernenen Objekte gewaschen werden und der Schmutz vielfältig sind, ist das Waschen ein sehr komplexer Prozess und der Grundprozess des Waschens kann in den folgenden einfachen Beziehungen ausgedrückt werden.
Carrie ·· Dirt + Waschmittel = Träger + Schmutz · Waschmittel
Der Waschprozess kann normalerweise in zwei Phasen unterteilt werden: Erstens wird der Schmutz unter der Wirkung des Waschmittels von seinem Träger getrennt; Zweitens wird der abgelöste Schmutz verteilt und im Medium suspendiert. Der Waschprozess ist ein reversibler Prozess, und der im Medium dispergierte und suspendierte Schmutz kann auch von dem Medium zum gewaschenen Objekt neu ausgeprägt werden. Daher sollte ein gutes Reinigungsmittel die Fähigkeit haben, Schmutz zu zerstreuen und zu suspendieren und Schmutz zu verhindern, zusätzlich zu der Fähigkeit, Schmutz aus dem Träger zu entfernen.
(1) Schmutzarten
Selbst für denselben Artikel können die Art, die Komposition und die Menge des Schmutzes je nach Umgebung variieren, in der er verwendet wird. Ölkörperdreck ist hauptsächlich einige tierische und pflanzliche Öle und Mineralöle (wie Rohöl, Heizöl, Kohle -Teer usw.), fester Schmutz ist hauptsächlich Ruß, Asche, Rost, Carbonschwarz usw. In Bezug auf Kleidung Dreck gibt es Schmutz aus dem menschlichen Körper, wie Schweiß, Sebum, Blut usw.; Schmutz aus Lebensmitteln wie Fruchtflecken, Speiseölflecken, Gewürzflecken, Stärke usw.; Dreck aus Kosmetika wie Lippenstift, Nagellack usw.; Dreck aus der Atmosphäre wie Ruß, Staub, Schlamm usw.; Andere, wie Tinte, Tee, Beschichtung usw. Es kommt in verschiedenen Arten.
Die verschiedenen Arten von Schmutz können normalerweise in drei Hauptkategorien unterteilt werden: fester Schmutz, flüssiges Schmutz und Spezialdreck.
① Festes Schmutz
Häufiger fester Schmutz umfasst Partikel aus Asche, Schlamm, Erde, Rost und Carbonschwarz. Die meisten dieser Partikel haben eine elektrische Ladung auf ihrer Oberfläche, die meisten von ihnen sind negativ aufgeladen und können leicht an Fasergegenständen adsorbiert werden. Ein fester Schmutz ist im Allgemeinen schwer in Wasser aufzulösen, kann jedoch durch Waschmittellösungen verteilt und aufgehängt werden. Ein fester Schmutz mit kleinerem Massenpunkt ist schwieriger zu entfernen.
② Flüssiger Schmutz
Flüssiger Schmutz ist größtenteils öllöslich, einschließlich Pflanzen- und Tiereöle, Fettsäuren, Fettalkoholen, Mineralölen und deren Oxiden. Unter ihnen können Pflanzen- und Tiereöle, Fettsäuren und Alkali -Saponifikation auftreten, während fetthaltige Alkohole, Mineralöle nicht durch Alkali saponifiziert werden, sondern in Alkoholkörpern, Ethers und Kohlenwasserstoff -organischen Lösungsmitteln sowie der Emulsifizierung und Streuung der Wasserlösung löslich sein können. Öllöslicher flüssiger Schmutz hat im Allgemeinen eine starke Kraft mit Fasergegenständen und wird an Fasern stärker adsorbiert.
③ Spezialdreck
Spezielle Schmutz umfasst Proteine, Stärke, Blut, menschliche Sekrete wie Schweiß, Talg, Urin und Fruchtsaft und Teesaft. Der größte Teil dieser Art von Schmutz kann chemisch und stark an Fasergegenständen adsorbiert werden. Daher ist es schwierig zu waschen.
Die verschiedenen Arten von Schmutz werden selten allein gefunden, aber oft miteinander gemischt und auf das Objekt adsorbiert. Schmutz kann manchmal unter externen Einflüssen oxidiert, zersetzt oder verfallen werden, wodurch neuen Schmutz erzeugt werden.
(2) Adhäsion von Schmutz
Kleidung, Hände usw. können befleckt werden, da zwischen dem Objekt und dem Schmutz eine Art Interaktion besteht. Schmutz haftet auf verschiedene Weise an Objekte, aber es gibt nur physikalische und chemische Adhäsionen.
①Die Haftung von Ruß, Staub, Schlamm, Sand und Holzkohle an Kleidung ist eine physische Haftung. Im Allgemeinen ist durch diese Adhäsion von Schmutz und die Rolle zwischen dem gefärbten Objekt relativ schwach, die Entfernung von Schmutz ist ebenfalls relativ einfach. Nach den verschiedenen Kräften kann die physikalische Adhäsion von Schmutz in eine mechanische Adhäsion und elektrostatische Adhäsion unterteilt werden.
A: Mechanische Haftung
Diese Art von Haftung bezieht sich hauptsächlich auf die Haftung eines festen Schmutzes (z. B. Staub, Schlamm und Sand). Die mechanische Adhäsion ist eine der schwächeren Formen der Schmutzversorgung und kann fast mit rein mechanischen Mitteln entfernt werden. Wenn der Schmutz jedoch klein ist (<0,1um), ist es schwieriger zu entfernen.
B: Elektrostatische Haftung
Die elektrostatische Adhäsion zeigt sich hauptsächlich in der Wirkung geladener Schmutzpartikel auf entgegengesetzt geladenen Objekten. Die meisten faserigen Objekte werden in Wasser negativ aufgeladen und können durch bestimmte positiv geladene Schmutz wie Kalktypen leicht eingehalten werden. Einige Schmutz, obwohl negativ geladen, wie z. B. CO2-Schwarzpartikel in wässrigen Lösungen, können sich durch ionische Brücken (Ionen zwischen mehreren entgegengesetzt geladenen Objekten, zusammen mit ihnen auf brückenähnliche Weise) an Fasern haften, die durch positive Ionen in Wasser (z. B. Ca2+ , mg2+ usw.) gebildet werden.
Die elektrostatische Wirkung ist stärker als die einfache mechanische Wirkung, wodurch die Schmutzentfernung relativ schwierig wird.
② Chemische Adhäsion
Die chemische Adhäsion bezieht sich auf das Phänomen von Schmutz, das durch chemische oder Wasserstoffbrückenbindungen auf ein Objekt wirkt. Zum Beispiel sind polare feste Schmutz, Protein, Rost und andere Adhäsion an Fasergegenständen, Fasern Carboxyl, Hydroxyl, Amid und andere Gruppen, diese Gruppen und fettige Schmutzfettsäuren, Fettalkohole sind leicht zu bilden Wasserstoffbindungen. Die chemischen Kräfte sind im Allgemeinen stark und der Schmutz ist daher fester mit dem Objekt verbunden. Diese Art von Schmutz ist mit den üblichen Methoden schwer zu entfernen und erfordert spezielle Methoden, um damit umzugehen.
Der Grad der Haftung von Schmutz hängt mit der Natur des Schmutzes und der Natur des Objekts zusammen, an das er eingehalten wird. Im Allgemeinen haften Partikel leicht an faserigen Gegenständen. Je kleiner die Textur des festen Schmutzes ist, desto stärker ist die Haftung. Polarer Schmutz an hydrophilen Objekten wie Baumwolle und Glas haften stärker als unpolarer Schmutz. Nicht-Polar-Schmutz haften stärker als polare Schmutz, wie polare Fette, Staub und Ton und sind weniger leicht zu entfernen und zu reinigen.
(3) Mechanismus zur Entfernung des Schmutzs
Der Zweck des Waschens ist es, Schmutz zu entfernen. In einem Medium einer bestimmten Temperatur (hauptsächlich Wasser). Unter Verwendung der verschiedenen physikalischen und chemischen Wirkungen des Waschmittels, um die Wirkung von Schmutz und gewaschenen Objekten zu schwächen oder zu beseitigen, unter der Wirkung bestimmter mechanischer Kräfte (wie Handabliebe, Waschmaschine Agitation, Wasseraufprall), so dass der Schmutz und die gewaschenen Objekte vom Zweck der Dekontamination.
① Mechanismus der Entfernung flüssiger Schmutz
A: Benetzung
Flüssigverschmutzung ist größtenteils auf Ölbasis. Öl färbt die meisten faserigen Gegenstände nass und verteilen Sie sich mehr oder weniger als Ölfilm auf der Oberfläche des faserigen Materials. Der erste Schritt in der Waschwirkung ist die Benetzung der Oberfläche durch die Waschflüssigkeit. Aus Gründen der Illustration kann die Oberfläche einer Faser als glatte feste Oberfläche betrachtet werden.
B: Ölablösung - Lockenmechanismus
Der zweite Schritt bei der Waschbewegung ist die Entfernung von Öl und Fett, die Entfernung von flüssigem Schmutz wird durch eine Art Spicks erreicht. Der flüssige Schmutz existierte ursprünglich auf der Oberfläche in Form eines verteilten Ölfilms, und unter der bevorzugten Benetzung der Waschflüssigkeit auf der festen Oberfläche (dh der Faseroberfläche) rollte er Schritt für Schritt in Ölperlen, die durch die Waschflüssigkeit ersetzt wurden und schließlich die Oberfläche unter bestimmten externen Kräften verließen.
② Mechanismus der festen Schmutzentfernung
Die Entfernung von flüssigem Schmutz erfolgt hauptsächlich durch die bevorzugte Benetzung des Schmutzträgers durch die Waschlösung, während der Entfernungsmechanismus für feste Schmutz unterschiedlich ist, wobei der Waschprozess hauptsächlich um die Benetzung der Schmutzmasse und ihre Trägeroberfläche durch die Waschlösung geht. Aufgrund der Adsorption von Tensiden am festen Schmutz und seiner Trägeroberfläche ist die Wechselwirkung zwischen dem Schmutz und der Oberfläche verringert und die Adhäsionsstärke der Schmutzmasse auf der Oberfläche reduziert, sodass die Schmutzmasse leicht von der Oberfläche des Trägers entfernt wird.
Darüber hinaus hat die Adsorption von Tensiden, insbesondere ionischen Tensiden, auf der Oberfläche des festen Schmutzes und seines Trägers das Potenzial, das Oberflächenpotential auf der Oberfläche des festen Schmutzes und seines Trägers zu erhöhen, was für die Entfernung des Schmutzs förderlicher ist. Feste oder allgemein faserige Oberflächen werden normalerweise in wässrigen Medien negativ aufgeladen und können daher diffuse doppelte elektronische Schichten auf Schmutzmassen oder festen Oberflächen bilden. Aufgrund der Abstoßung homogener Ladungen wird die Adhäsion von Schmutzpartikeln im Wasser an die feste Oberfläche geschwächt. Wenn ein anionisches Tensid hinzugefügt wird, da es gleichzeitig das negative Oberflächenpotential des Schmutzpartikels und der festen Oberfläche erhöhen kann, ist die Abstoßung zwischen ihnen verstärkt, die Adhäsionsstärke des Partikels ist stärker und der Schmutz ist leichter zu entfernen.
Nichtionische Tenside werden auf allgemein geladenen festen Oberflächen adsorbiert, und obwohl sie das Grenzflächenpotential nicht signifikant verändern, neigen die adsorbierten nichtionischen Tenside dazu, eine bestimmte Dicke der adsorbierten Schicht auf der Oberfläche zu bilden, die zur Vorbeugung der Wiedereinlagerung von Schmutz hilft.
Bei kationischen Tensiden reduziert oder eliminiert ihre Adsorption das negative Oberflächenpotential der Schmutzmasse und ihrer Trägeroberfläche, wodurch die Abstoßung zwischen Schmutz und Oberfläche verringert wird und daher der Entfernung der Schmutz nicht förderlich ist. Nach der Adsorption an der festen Oberfläche neigen kationische Tenside dazu, die feste Oberfläche hydrophoben zu drehen, und sind daher nicht der Oberflächenbenetzung und waschen nicht förderlich.
③ Entfernung spezieller Böden
Protein, Stärke, menschliche Sekrete, Fruchtsaft, Teesaft und andere solche Schmutz sind mit normalen Tensiden schwer zu entfernen und erfordern eine besondere Behandlung.
Proteinflecken wie Creme, Eier, Blut, Milch und Hautausscheidung tendenziell an den Fasern und Degeneration tendenziell koagulieren und eine stärkere Haftung erhalten. Proteinverschmutzung kann unter Verwendung von Proteasen entfernt werden. Die Enzymprotease zerlegt die Proteine im Schmutz in wasserlösliche Aminosäuren oder Oligopeptide.
Stärkeflecken stammen hauptsächlich aus Lebensmitteln, andere wie Soße, Kleber usw. Amylase hat einen katalytischen Effekt auf die Hydrolyse von Stärkeflecken, wodurch Stärke in Zucker zusammenbricht.
Lipase katalysiert die Zersetzung von Triglyceriden, die mit normalen Methoden wie Talg- und essbarer Ölen schwer zu entfernen sind und sie in lösliche Glycerin- und Fettsäuren unterbreiten.
Einige farbige Flecken von Fruchtsäften, Tee -Säften, Tinten, Lippenstift usw. sind selbst nach wiederholtem Waschen oft schwierig zu reinigen. Diese Flecken können durch eine Redoxreaktion mit einem oxidierenden oder reduzierenden Mittel wie Bleichmittel entfernt werden, das die Struktur der farbgenerierenden oder farbigen Fachgruppen zerstört und sie in kleinere wasserlösliche Komponenten beeinträchtigt.
(4) Fleckenentfernungsmechanismus der trockenen Reinigung
Das obige ist eigentlich für Wasser als das Waschenmedium. Tatsächlich ist aufgrund der verschiedenen Arten von Kleidung und Struktur eine gewisse Kleidung mit Wasserwäsche nicht bequem oder nicht leicht zu waschen, etwas Kleidung nach dem Waschen und sogar Verformung, Verblassen usw., zum Beispiel: Die meisten natürlichen Fasern absorbieren Wasser und leicht zu schwellen und trocken und leicht zu schrumpfen, so dass nach dem Waschen deformiert wird. Durch das Waschen von Wollprodukten erscheinen auch häufig ein Schrumpfungsphänomen, einige Wollprodukte mit Wasserwäsche sind auch leicht zu pillen, Farbwechsel. Einige Seiden Handgefühl werden nach dem Waschen und verlieren ihren Glanz schlechter. Für diese Kleidung verwenden Sie häufig die Trockenreinigungsmethode, um zu dekontaminieren. Die sogenannte trockene Reinigung bezieht sich im Allgemeinen auf die Waschmethode in organischen Lösungsmitteln, insbesondere in nicht-polaren Lösungsmitteln.
Die chemische Reinigung ist eine sanftere Form des Waschens als Wasserwäsche. Da die chemische Reinigung nicht viel mechanische Wirkung erfordert, verursacht sie keine Beschädigungen, Falten und Verformungen der Kleidung, während die trockenen Reinigungsmittel im Gegensatz zu Wasser selten Expansion und Kontraktion erzeugen. Solange die Technologie ordnungsgemäß behandelt wird, kann die Kleidung ohne Verzerrung, das Verblassen und die Lebensdauer der Lebensdauer trocken gereinigt werden.
In Bezug auf die trockene Reinigung gibt es drei breite Arten von Schmutz.
①oillösliche schmutzöl-lösliche Schmutz umfasst alle Arten von Öl und Fett, die flüssig oder fettig sind und in trockenen Reinigungslösungsmitteln gelöst werden können.
② Wasserlöslicher Schmutz wasserlöslicher Schmutz ist in wässrigen Lösungen löslich, jedoch nicht in trockenen Reinigungsmitteln, wird in einem wässrigen Zustand an Kleidung adsorbiert, verdampft Wasser nach dem Ausfall von körnigen Feststoffen wie anorganischen Salzen, Stärke, Protein usw. usw.
③oil- und Wasser unlösliches Schmutzöl und Wasser unlöslicher Schmutz sind weder löslich in Wasser noch löslich in trockenen Reinigungslösungsmitteln wie Carbonschwarz, Silikate verschiedener Metalle und Oxide usw.
Aufgrund der unterschiedlichen Natur verschiedener Arten von Schmutz gibt es verschiedene Möglichkeiten, Schmutz im Trockenreinigungsprozess zu entfernen. Öllösliche Böden wie tierische und pflanzliche Öle, Mineralöle und Fettsäuren sind in organischen Lösungsmitteln leicht löslich und können in der trockenen Reinigung leichter entfernt werden. Die hervorragende Löslichkeit von Trockenreinigungslösungsmitteln für Öle und Fetten kommt im Wesentlichen von den Van der Wänden zwischen Molekülen.
Für die Entfernung von wasserlöslichen Schmutz wie anorganische Salze, Zucker, Proteine und Schweiß muss auch die richtige Menge Wasser zum trockenen Verringerungsmittel hinzugefügt werden, ansonsten ist wasserlöslicher Schmutz schwer aus der Kleidung zu entfernen. Wasser ist jedoch schwer im Trockenreinigungsmittel aufzulösen. Um die Wassermenge zu erhöhen, müssen Sie auch Tenside hinzufügen. Das Vorhandensein von Wasser im Trockenreinigungsmittel kann die Oberfläche des Schmutzes und der Kleidung hydratisiert machen, so dass es leicht ist, mit den polaren Gruppen von Tensiden zu interagieren, was der Adsorption von Tensiden auf der Oberfläche förderlich ist. Wenn Tenside Mizellen bilden, können wasserlösliche Schmutz und Wasser in die Mizellen lockisiert werden. Tenside können nicht nur den Wassergehalt des Trockenreinigungsmittels erhöhen, sondern auch eine Rolle bei der Verhinderung der Neuauflage von Schmutz spielen, um den Dekontaminationseffekt zu verbessern.
Das Vorhandensein einer geringen Menge Wasser ist erforderlich, um wasserlösliche Schmutz zu entfernen, aber zu viel Wasser kann zu Verzerrungen und Falten in einigen Kleidung führen, sodass die Menge an Wasser im trockenen Verringerungsmittel gemäßigt sein muss.
Schmutz, der weder wasserlöslich noch öllösliche, feste Partikel wie Asche, Schlamm, Erde und Carbonschwarz ist, wird im Allgemeinen durch elektrostatische Kräfte oder in Kombination mit Öl am Kleidungsstück befestigt. Bei der trockenen Reinigung kann der Aufprall der Lösungsmittelabfluss die elektrostatische Kraft-Adsorption von Schmutz ausschalten, und trockener Reinbarungsmittel kann das Öl auflösen, sodass die Kombination von Öl und Schmutz und an der Kleidung von festen Partikeln in der trockenen Verringerung des Trockenreinigungsmittels an der Kleidung von festen Partikeln im trockenen Abzweifungsmittel in einer kleinen Menge an Wasser und deren, die sich verhindern. Kleidung.
(5) Faktoren, die sich auf das Waschanlagen auswirken
Die gerichtete Adsorption von Tensiden an der Grenzfläche und die Verringerung der Oberflächenspannung sind die Hauptfaktoren bei der Entfernung von flüssigem oder festem Schmutz. Der Waschprozess ist jedoch komplex und der Wascheffekt wird, auch wenn der gleiche Waschmitteltyp, von vielen anderen Faktoren beeinflusst wird. Diese Faktoren umfassen die Konzentration des Reinigungsmittels, die Temperatur, die Art der Verschmutzung, die Art der Faser und die Struktur des Stoffes.
① Tensidkonzentration
Die Mizellen von Tensiden in Lösung spielen eine wichtige Rolle im Waschprozess. Wenn die Konzentration die kritische Mizellenkonzentration (CMC) erreicht, nimmt der Wascheffekt stark zu. Daher sollte die Konzentration des Reinigungsmittels im Lösungsmittel höher sein als der CMC -Wert, um eine gute Waschwirkung zu haben. Wenn jedoch die Konzentration des Tensids höher ist als der CMC -Wert, ist die inkrementelle Zunahme des Waschmittels nicht offensichtlich und es ist nicht erforderlich, die Konzentration des Tensids zu stark zu erhöhen.
Beim Entfernen von Öl durch Solubilisierung nimmt der Solubilisierungseffekt mit zunehmender Tensidkonzentration zu, selbst wenn die Konzentration über CMC liegt. Zu diesem Zeitpunkt ist es ratsam, Waschmittel auf lokale zentralisierte Weise zu verwenden. Wenn beispielsweise viel Schmutz auf den Manschetten und einem Kleidungskragen eines Kleidungsstücks vorhanden ist, kann während des Waschens eine Waschmittelschicht aufgetragen werden, um den solubilisierenden Effekt des Tensids auf das Öl zu erhöhen.
Die Temperatur hat einen sehr wichtigen Einfluss auf die Dekontaminationsaktion. Im Allgemeinen erleichtert die Erhöhung der Temperatur die Entfernung von Schmutz, aber manchmal kann eine zu hohe Temperatur auch zu Nachteilen führen.
Der Temperaturanstieg erleichtert die Diffusion von Schmutz, festes Fett ist bei Temperaturen über seinem Schmelzpunkt leicht emulgiert und die Fasern erhöhen sich aufgrund der Temperaturzunahme, die alle die Entfernung von Schmutz erleichtern. Für kompakte Stoffe werden die Mikrogaps zwischen den Fasern jedoch reduziert, wenn sich die Fasern ausdehnen, was für die Entfernung von Schmutz schädlich ist.
Temperaturänderungen beeinflussen auch die Löslichkeit, den CMC -Wert und die Mizellengröße von Tensiden, wodurch der Wascheffekt beeinflusst wird. Die Löslichkeit von Tensiden mit langen Kohlenstoffketten ist bei niedrigen Temperaturen niedrig und manchmal ist die Löslichkeit noch niedriger als der CMC -Wert, sodass die Waschtemperatur angemessen angehoben werden sollte. Der Effekt der Temperatur auf den CMC-Wert und die Mizellengröße unterscheidet sich für ionische und nichtionische Tenside. Bei ionischen Tensiden erhöht ein Temperaturanstieg im Allgemeinen den CMC -Wert und verringert die Mizellengröße, was bedeutet, dass die Konzentration des Tensids in der Waschlösung erhöht werden sollte. Bei nichtionischen Tensiden führt ein Temperaturanstieg zu einer Verringerung des CMC-Werts und zu einem signifikanten Anstieg des Mizellenvolumens. Daher ist klar, dass ein angemessener Temperaturanstieg dem nichtionischen Tensid dazu beiträgt, seinen oberflächenaktiven Effekt auszuüben. Die Temperatur sollte jedoch ihren Wolkenpunkt nicht überschreiten.
Kurz gesagt, die optimale Waschtemperatur hängt von der Waschmittelformulierung und dem gewaschenen Objekt ab. Einige Reinigungsmittel haben einen guten Waschmitteleffekt bei Raumtemperatur, während andere eine ganz andere Waschung zwischen kaltem und heißem Waschen haben.
③ Schaum
Es ist üblich, die Schaumkraft mit Waschwirkung zu verwirren, und glaubt, dass Waschmittel mit hoher Schäumung eine gute Waschwirkung haben. Untersuchungen haben gezeigt, dass es keinen direkten Zusammenhang zwischen dem Wascheffekt und der Menge an Schaum gibt. Zum Beispiel ist das Waschen mit geringen Schaumwaschmitteln nicht weniger wirksam als das Waschen mit hohen Schaumwaschmitteln.
Obwohl der Schaum nicht direkt mit dem Waschen zusammenhängt, gibt es Anlässe, wenn er zum Beispiel beim Entfernen von Schmutz beim Waschen von Schalen von Hand hilft. Wenn Sie Teppiche schrubben, kann der Schaum auch Staub und andere feste Schmutzpartikel wegnehmen. Teppichschmutz verantwortlich für einen großen Teil des Staubes, sodass die Teppichreinigungsmittel eine bestimmte Schaumstofffähigkeit haben sollten.
Die Schaumkraft ist auch für Shampoos wichtig, wo der feine, der von der Flüssigkeit während des Shampoonierens oder des Bades erzeugte feine Schaumstoff, das die Haare geschmiert und komfortabel lässt.
④ Sorten von Fasern und physikalischen Eigenschaften von Textilien
Zusätzlich zur chemischen Struktur der Fasern, die die Adhäsion und Entfernung von Schmutz beeinflusst, beeinflussen das Erscheinungsbild der Fasern und die Organisation des Garns und des Stoffes einen Einfluss auf die Leichtigkeit der Schmutzentfernung.
Die Skalen von Wollfasern und die gekrümmten flachen Bänder von Baumwollfasern sammeln häufiger Schmutz als glatte Fasern an. Zum Beispiel ist bei Cellulosefilmen (Viskosefilme), die auf Cellulosefilmen gefärbt sind, leicht zu entfernen, während auf Baumwollstoffe gefärbte Carbonschwarz schwer zu waschen ist. Ein weiteres Beispiel ist, dass Kurzfaserstoffe aus Polyester anfälliger für die Ansammlung von Ölflecken sind als langfaserstoffe, und Ölflecken auf Kurzfasern sind ebenfalls schwieriger zu entfernen als Ölflecken auf langfaseren Stoffen.
Aufgrund der geringen Lücke zwischen den Fasern können eng verdrehte Garne und enge Stoffe der Invasion von Schmutz widerstehen, aber das Gleiche kann auch verhindern, dass die Wäscheflüssigkeit den inneren Schmutz ausschließt, sodass enge Stoffe dem Schmutz gut widerstehen, aber wenn das Waschen des Bothots auch nach dem Waschen des Beinens schwieriger ist.
⑤ Wasserhärte
Die Konzentration von Ca2+, Mg2+ und anderen Metallionen im Wasser hat einen großen Einfluss auf die Waschwirkung, insbesondere wenn die anionischen Tenside Ca2+ und Mg2+ -Ionen begegnen, die Calcium- und Magnesiumsalze bilden, die weniger löslich sind und ihre Wünsche verringern. In hartem Wasser ist die Waschität immer noch viel schlechter als bei der Destillation, selbst wenn die Konzentration des Tensids hoch ist. Damit das Tensid die beste Waschwirkung aufweist, sollte die Konzentration von Ca2+ -Ionen im Wasser auf 1 x 10-6 mol/l (CACO3 auf 0,1 mg/l) oder weniger reduziert werden. Dies erfordert die Zugabe verschiedener Enthärter zum Waschmittel.
Postzeit: Februar-25-2022



